Τράπεζα Θεμάτων
www.trapeza-thematon.gr
| Τύπος Σχολείου: | Γενικό Λύκειο | Τάξη: | Α' Λυκείου |
|---|---|---|---|
| Μάθημα: | Χημεία | Θέμα: | 2 |
| Κωδικός Θέματος: | 38879 | Ύλη: | 2.1.2 Κατανομή ηλεκτρονίων σε στιβάδες 2.3.5 Ιοντικός ή ετεροπολικός δεσμός 2.3.6 Χαρακτηριστικά ιοντικών ή ετεροπολικών ενώσεων |
| Τύπος Σχολείου: | Γενικό Λύκειο |
|---|---|
| Τάξη: | Α' Λυκείου |
| Μάθημα: | Χημεία |
| Θέμα: | 2 |
| Κωδικός Θέματος: | 38879 |
| Ύλη: | 2.1.2 Κατανομή ηλεκτρονίων σε στιβάδες 2.3.5 Ιοντικός ή ετεροπολικός δεσμός 2.3.6 Χαρακτηριστικά ιοντικών ή ετεροπολικών ενώσεων |
| Τελευταία Ενημέρωση: 17-Δεκ-2025 | |
Θέμα 2ο
2.1 Σε μια τάξη η καθηγήτρια Χημείας καλεί τους μαθητές και τις μαθήτριές της να βρουν έναν τρόπο να μετρήσουν την άγνωστη συγκέντρωση ενός διαλύματος \(NaCl\). Μια ομάδα μαθητών/ριών πρότεινε την ακόλουθη λύση: να κατασκευάσει μια συσκευή ανίχνευσης της αγωγιμότητας ενός διαλύματος, αποτελούμενη από ηλεκτρική πηγή, αμπερόμετρο και καλώδια (Σχήμα 1).

Στη συνέχεια, να παρασκευάσει επτά (7) διαλύματα \(NaCl\) με διαφορετικές συγκεντρώσεις και να μετρήσει την ένταση του ρεύματος που διαπερνά το κάθε διάλυμα. Τέλος, να μετρήσει την ένταση του ρεύματος που διαπερνά το διάλυμα άγνωστης συγκέντρωσης και μέσω της γραφικής παράστασης της σχέσης έντασης ρεύματος – συγκέντρωσης \(NaCl\) να υπολογίσει την άγνωστη συγκέντρωση.
α) Για ποιον λόγο τα υδατικά διαλύματα του \(NaCl\) είναι αγώγιμα;
(Μονάδες 3)
β) Αναμένετε ότι τα διαλύματα με τη μεγαλύτερη συγκέντρωση του άλατος θα δίνουν υψηλότερες ή χαμηλότερες τιμές έντασης του ηλεκτρικού ρεύματος;
(Μονάδες 3)
γ) Τα παιδιά εκτελώντας τα πειράματά τους, έλαβαν τις σχετικές πειραματικές τιμές και σχεδίασαν τη γραφική παράσταση της σχέσης έντασης ρεύματος – συγκέντρωσης (Σχήμα 2).
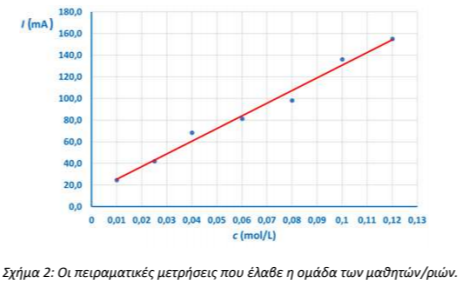
Με βάση το παραπάνω γράφημα, διαπιστώνετε κάποια σχέση ανάμεσα στη συγκέντρωση του διαλύματος και την ένταση του ρεύματος; Να αιτιολογήσετε την απάντησή σας.
(Μονάδες 3)
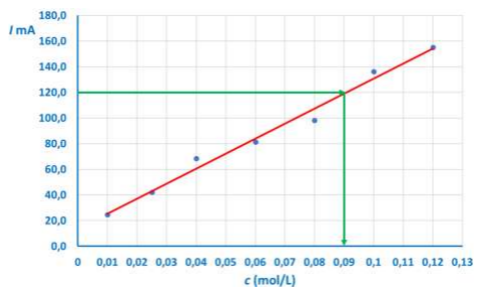
δ) Μπορείτε να εξηγήσετε στους μαθητές/τριες ποια είναι η συγκέντρωση του διερευνώμενου διαλύματος \(NaCl\), αν γνωρίζετε ότι η ένταση του ρεύματος που έδειξε το αμπερόμετρο κατά τη μέτρηση ήταν \(120,0 mA\).
(Μονάδες 3)
Μονάδες 12
2.2 Οι ιοντικές ενώσεις αναπτύσσονται σε κρυσταλλικά πλέγματα. Οι ενώσεις \(NaF\) και \(MgF\) σχηματίζουν και οι δύο κυβικό κρυσταλλικό πλέγμα (χαρακτηριστικό παράδειγμα κυβικού κρυσταλλικού πλέγματος αποτελεί το \(NaCl\)), όπως φαίνεται στο Σχήμα 3.
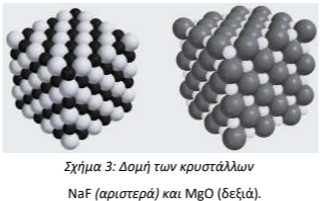
Δίνονται: \(Ζ(Νa)=11\), \(Ζ (F)=9\), \(Ζ (Mg)=12\) και \(Ζ (O)=8\).
α) Να γράψετε την ηλεκτρονιακή δομή των ιόντων \(Μg^{2+}\) και \(O^{2-}\).
(Μονάδες 2)
β) Να εξηγήσετε ποια σωματίδια αναπαριστούν οι μεγάλες και ποια οι μικρές σφαίρες στον κρύσταλλο του \(MgO\).
(Μονάδες 4)
γ) Στο παρακάτω σχήμα φαίνεται μια διατομή του κρυσταλλικού πλέγματος του \(NaF\).
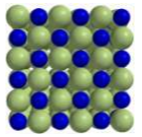
Σε μια τάξη Α' Λυκείου ένας μαθητής και μια μαθήτρια διαφωνούν παρατηρώντας αυτό το σχήμα. Ο Αναξίμανδρος υποστηρίζει ότι «το κάθε ιόν νατρίου συνδέεται μόνο με ένα ιόν φθορίου, αυτό στο οποίο εκχώρησε το ηλεκτρόνιό του». Η Υπατία του απαντά ότι «κάθε ιόν νατρίου σχηματίζει 6 ιοντικούς δεσμούς με τα άμεσα γειτονικά του ιόντα». Ποιος από τους δύο μαθητές έχει δίκιο; Να εξηγήσετε την απάντησή σας.
(Μονάδες 3)
δ) Το σημείο τήξεως του \(NaF\) είναι \(993 °C\), ενώ του \(MgO\) είναι \(2.852 °C\). Μπορείτε να εξηγήσετε γιατί υπάρχει τόσο μεγάλη διαφορά ανάμεσα στα δύο σημεία τήξεως;
(Μονάδες 4)
Μονάδες 13
Το παραπάνω θέμα αναπτύχθηκε στο πλαίσιο του έργου: «Ανάπτυξη Δοκιμασιών Αξιολόγησης Δεξιοτήτων Εγγραμματισμού στα μαθήματα της Νεοελληνικής Γλώσσας και Λογοτεχνίας, της Άλγεβρας, της Φυσικής και της Χημείας Α’ Λυκείου Γενικού Λυκείου» Ανάδοχος: «Ειδικός Λογαριασμός Κονδυλίων Έρευνας (Ε.Λ.Κ.Ε) Πανεπιστημίου Ιωαννίνων» ΑΔΑΜ: 25SYMV016348911 2025-02-20.
Απάντηση Θέματος:
Ενδεικτικές Απαντήσεις
2.1
α) Το \(NaCl\) αποτελεί ιοντική ένωση. Κατά τη διάλυση των ιοντικών ενώσεων στο νερό, τα πολικά μόρια του νερού απομακρύνουν τα ιόντα από τον κρύσταλλο και τα ιόντα αυτά κινούνται ελεύθερα στο διάλυμα. Έτσι, για το NaCl έχουμε:
\(NaCl(s) \rightarrow Na^+(aq) + Cl^-(aq)\).
β) Μεγαλύτερη συγκέντρωση του άλατος σημαίνει μεγαλύτερη συγκέντρωση ιόντων, δηλαδή φορέων του ηλεκτρικού ρεύματος. Επομένως, περιμένουμε υψηλότερες τιμές έντασης του ηλεκτρικού ρεύματος.
γ) Από την προσαρμογή των πειραματικών τιμών, που έγινε με τη χάραξη της κόκκινης γραμμής, προκύπτει ότι η ένταση του ρεύματος αυξάνεται γραμμικά σε σχέση με τη συγκέντρωση του άλατος. Επομένως, όσο αυξάνεται η συγκέντρωση του άλατος, αυξάνεται ανάλογα και η ένταση του ρεύματος.
δ) Αφού τα ποσά είναι ανάλογα, από το διάγραμμα προκύπτει ότι για τιμή ρεύματος 120,0 mA η συγκέντρωση του \(NaCl\) θα είναι \(0,09 Μ\).
2.2
α) \(_{12}Mg\): \(K(2) L(8) M(2)\), άρα για το κατιόν με φορτίο \(2+\) έχουμε: \(_{12}Mg^{2+}\): \(K(2) L(8)\).
\(_8Ο\): \(K(2) L(6)\), άρα για το ανιόν με φορτίο \(2-\) έχουμε: \(_8Ο^{2-}\): \(K(2) L(8)\).
β) Τα δυο ιόντα έχουν την ίδια ηλεκτρονιακή δομή. Όμως, τα \(10\) ηλεκτρόνια του κατιόντος έλκονται από τα \(12\) πρωτόνια του πυρήνα του μαγνησίου, ενώ τα \(10\) ηλεκτρόνια του ανιόντος έλκονται από τα \(8\) πρωτόνια του πυρήνα του οξυγόνου. Επομένως, αναμένεται το μέγεθος του κατιόντος να είναι αρκετά μικρότερο από αυτό του ανιόντος, οπότε οι μεγάλες σφαίρες απεικονίζουν τα ιόντα \(O^{2-}\), ενώ οι μικρές σφαίρες τα ιόντα \(Mg^{2+}\).
γ) Όπως φαίνεται και στα σχήματα, κάθε θετικό ιόν (οι μικρότερες σφαίρες) στον κρύσταλλο του άλατος έχει στην άμεση γειτονιά του \(6\) ανιόντα (οι μεγαλύτερες σφαίρες). Τα ανιόντα είναι \(6\), διότι πέρα από τα τέσσερα (\(4\)) που φαίνονται (πάνω, κάτω, δεξιά και αριστερά), υπάρχει ένα ανιόν μπροστά από το επίπεδο και ένα ακόμα πίσω από αυτό. Άρα η Υπατία έχει δίκιο.
δ) Τα ιόντα συγκρατούνται στον κρύσταλλο με ισχυρές δυνάμεις Coulomb. Οι δυνάμεις Coulomb είναι ανάλογες με το μέγεθος των φορτίων των ιόντων (ενώ μειώνονται με το τετράγωνο της μεταξύ τους απόστασης). Στο \(MgO\) τα ιόντα έχουν φορτίο \(2+\) και \(2-\), ενώ στο \(NaF\) έχουν φορτίο \(1+\) και \(1-\). Επομένως, τα μεγαλύτερα φορτία στο \(MgO\) δημιουργούν ισχυρότερες ελκτικές δυνάμεις μεταξύ των ιόντων, γεγονός που απαιτεί υψηλότερη θερμοκρασία, για να απομακρυνθούν τα ιόντα από τις θέσεις τους και να επέλθει η τήξη. Γι’ αυτό το \(MgO\) έχει πολύ μεγαλύτερο σημείο τήξεως από το \(NaF\).
Το θέμα προέρχεται και αντλήθηκε από την πλατφόρμα της Τράπεζας Θεμάτων Διαβαθμισμένης Δυσκολίας που αναπτύχθηκε (MIS5070818-Tράπεζα θεμάτων Διαβαθμισμένης Δυσκολίας για τη Δευτεροβάθμια Εκπαίδευση, Γενικό Λύκειο-ΕΠΑΛ) και είναι διαδικτυακά στο δικτυακό τόπο του Ινστιτούτου Εκπαιδευτικής Πολιτικής (Ι.Ε.Π.) στη διεύθυνση (http://iep.edu.gr/el/trapeza-thematon-arxiki-selida).